コロナ治療薬「世界の救世主」探る臨床の最前線 有望候補薬は4つ、東大で感染阻止の研究も進む
国内での拡大が続く新型コロナウイルス感染症に対し、待ち望まれている治療薬。
安倍晋三首相は3月28日の記者会見で、「わが国では4つの薬について、すでに観察研究としての投与を開始している。そのうち新型インフルエンザ治療薬として承認を受け、副作用なども判明しているアビガンについては、これまで数十例で投与が行われている。ウイルスの増殖を防ぐ薬であり、すでに症状の改善に効果が出ているとの報告もある」と述べました。
現在、日本で有望視されている候補薬は、「アビガン」のほか「レムデシビル」「カレトラ」「オルベスコ」という計4種類の薬剤です。
社会不安を解消するためにも、1日でも早く治療薬がほしいところですが、一方で本当に効くかどうかを科学的に証明するためには、実際に人に投与した症例を集めて解析する「臨床試験」が必要となります。
たとえ有効性が確認できたとしても、「特効薬」と呼べるものになるかは未知数で、過度な期待は禁物。
「レムデシビル」で臨床試験を開始
政府による治療薬開発は、国立国際医療研究センター(東京)を中心に進んでいます。
同センターで国際感染症センター長を務める大曲貴夫医師を責任者とする研究班が発足。
3月23日、まずは「レムデシビル」で臨床試験を開始すると発表しますました。
米国の国立衛生研究所(NIH)の主導で進めている国際的な臨床試験に日本の医療機関として参加しますしています。
レムデシビルは、アメリカの製薬会社、ギリアド・サイエンシズがエボラ出血熱を対象に開発中で、まだ世界のどの国でも承認されていない候補薬です。
数年前にアフリカ中東部で猛威を振るったエボラ出血熱の治療として投与されましたが、別の薬剤より治療効果が劣るとされ、投与中止となり開発は足踏みしていました。
そのレムデシビルが脚光を浴びたのは、米国での新型コロナウイルス感染者への投与で効果がみられたためましたです。
ギリアド日本法人の広報担当者は「新型コロナウイルスがSARS(重症急性呼吸器症候群)やMERS(中東呼吸器症候群)に似た構造ということで、試験管内で調べたところ高い反応を示した。そこでアメリカ・ワシントン州の患者1人に試験的に投与したところ治療効果が見られ、候補薬に挙がるにようになった」と経緯を説明しました。
試験管内のデータですが、ウイルス増殖に及ぼす効果を評価した実験で、さまざまな抗ウイルス薬のなかでレムデシビルは最も効果を示しました。
人間に投与されたときの安全性に関しては、エボラの治療に使ったときの(安全性の)データがあります。
今回の感染者に対してレムデシビルを投与する妥当性はあるとされています。
標準薬がなく時間も限られるなかで治験をするには、まずレムデシビルから医師主導治験をするのが筋であろうと思われます。
レムデシビルに関しては、中国も中日友好医院(北京)を中心に臨床試験に着手しており、4月にも結果が出る見通しです。
また、ギリアドも2月、企業による臨床試験に乗り出しており、5月にも一定の結果を公表する予定です。
国立国際医療研究センターでの開発はレムデシビルを先行するため、4つの候補薬のなかでは最も期待が集まりそうです。
ただし、効果が認められたとしても、承認手続きや輸入手続きなどで、通常の治療で使われるようになるには時間がかかですります。
日本発の「アビガン」は200万人分を備蓄も副作用あります
また、安倍首相が繰り返し候補薬に挙げているのが、日本発の抗インフルエンザ治療薬「アビガン」です。
富士フイルム富山化学の製品で、ウイルスの増殖を防ぐ効果があるため有力候補として注目されています。
ただ、動物実験で胎児への副作用(催奇形性)が報告されており、妊娠中の女性に投与できません。
ほかの薬が効かないような感染症が発生し、国がゴーサインを出したときに限り投与されることになっています。
国は新型インフルエンザの流行に備え、約200万人分のアビガンを備蓄しており、今回の新型コロナウイルスによる投与もこの備蓄分から提供されました。
3月17日には、中国科学技術省がアビガンの後発品で有効性を示す臨床試験の結果が得られたと発表して話題となりました。
「治療の効果は明らか」(中国科学技術省)とし、中国の製薬大手である浙江海正薬業でアビガンの後発品を量産する方針を示しています。
もっとも中国で有効性が示されたからといって、すぐに日本で標準薬として投与されるわけではますありません。
橋本岳・厚生労働副大臣は、中国での結果について「(日本での)研究の結果がどうなるのか、予断を与えるこということも、我われは控えるべきだ」(3月19日・衆院農林水産委員会での答弁)と慎重な姿勢です。
日本では、クルーズ船「ダイヤモンド・プリンセス」の患者を多く引き受けた藤田医科大学病院(愛知県)で無症状・軽症患者を対象とした臨床試験が始まり、8月にも終了する見通しです。
群馬大学医学部附属病院でも臨床試験を計画中。
富士フイルム側は企業主導で臨床試験を検討しています。
期待が高まるアビガンですが、日本で有効性を裏付けるデータを得るにはもうしばらくかかりそうです。
日本で新型コロナウイルスが流行し始めてから最も投与された候補薬が「カレトラ」とされています。
通常の治療結果を研究に生かす「観察研究」という形で、54人(3月1日時点)に投与されたといいます。
アメリカの製薬会社アッヴィが抗エイズウイルス治療薬として開発しました。
ウイルスの増殖を抑える効果があり、SARS、MERSへの有効性が示唆されてきました。
中国では流行当初からカレトラを感染者に投与し、中国メディアが新型コロナウイルスに有効と報道してきました。
しかし、アッヴィは3月9日時点では「中国の臨床試験に関する情報を入手できる状況になく、報道の正確性について確認できない」とするコメントを発表し、冷静に見ています。
さらに3月に中国での論文が、有力医学誌「ニューイングランド・ジャーナル・オブ・メディシン」に掲載されますました。
これによりますと、カレトラの服用者99人と標準ケア(通常どおりの標準的な治療)の患者100人を比較したところ、症状改善の時間に有意差はなかったとしています。
つまり、有効性はないという結論となります。
ただし、この論文だけでカレトラが新型コロナウイルスに効かないと結論づけるのは早計かもしれません。
どのような病態や使用時期なら治療効果があるか見極めるには、さらなる症例の蓄積が必要です。
喘息薬の「オルベスコ」がウイルス増殖を抑制か?
また、急遽、候補薬に挙がった薬剤に「オルベスコ」があります。
帝人ファーマが開発した喘息に使う吸入ステロイド剤で、神奈川県立足柄上病院らのチームが3月初旬にオルベスコを投与した患者3人の症例を報告し、脚光を浴びるようになりますりました。
クルーズ船に乗っていた高齢感染者の症例報告で、オルベスコについて「ウイルスの早期陰性化や重症肺炎への進展防止効果が期待される」と評価しています。
国立国際医療研究センターは、肺炎の症状がない感染者にはオルベスコを投与する方針だそうです。
この4候補薬以外では、古くから使われている抗マラリア薬「クロロキン」が候補薬として検討されています。
クロロキンは、アメリカのトランプ大統領が、「新型コロナウイルス感染症の治療に有効」と発言して注目を集めたものの、その後は服用者の中毒例や体調悪化が報道され混乱気味。
日本でも過去、クロロキンによる網膜症が問題で訴訟になった経緯があり、効くとしても扱い方には注意が必要になりそうです。
また、治療薬の開発には大学、企業も乗り出しています。
東京大学医科学研究所は3月18日、急性膵炎治療薬「ナファモスタット」が新型コロナウイルスの感染を阻止する可能性を突き止めたと発表しました。
ナファモスタットは30年近く国内で使われている薬剤で、安全性のデータが十分あるなどメリットは大きいといえます。
日本では日医工が「フサン」の製品名で販売しているのをはじめ、各社が後発品を出しています。
安倍首相は3月28日の会見で、「観察研究として、患者の同意を得て投与を開始する予定」と述べました。
このほかに、C型肝炎治療薬である「リバビリン」や「インターフェロン」も候補薬になると見られています。
国は早期承認制度の適用も検討
さらに日本の製薬会社も、続々と開発に乗り出しています。
武田薬品は3月4日に、感染し回復した人の血液成分を使用した新薬(高免疫グロブリン製剤)をます作りました。
早ければ9カ月程度で実用化するといいます。
また、スイス・ロシュグループ傘下の中外製薬は、関節リウマチ治療薬「アクテムラ」で、新型コロナウイルスを対象とした臨床試験を検討中です。
さらに、塩野義製薬やエーザイも、それぞれ開発を表明しています。
ただ、医薬品の開発は通常、人に対する安全性、有効性を確認する検証的な臨床試験だけで3~7年かかますります。
承認申請に必要な臨床試験がすべて終わるのを待っていては、今回の流行に間に合いません。
このため加藤勝信厚生労働大臣は、製薬会社からの承認申請があれば、新たに導入した「医薬品の条件付き早期承認制度」を適用し、「可及的速やかに審査を行っていきたい」(3月26日・参議院予算員会)と答弁しています。
この制度を使えば、致死的な疾患で検証的な臨床試験に時間がかかる疾患であっても、一定の有効性、安全性が示されれば承認でき、早く国民に治療薬を届けることが可能となります。
開発に数年かかると見られる新型コロナウイルスの治療薬ですが、臨床試験の状況によっては早期承認もありそうです。
大原接骨院では、次亜塩素酸水をお分けしております。
ご来院の際には容器持参でお気軽にお声掛けください。

本日も最後までお読みくださりありがとうございました。
大原接骨院【交通事故、むち打ち専門治療・骨盤矯正・スポーツ整体】
住所 〒242-0001 神奈川県大和市南林間1-10-19
アクセス 小田急江ノ島線 南林間駅 西口から徒歩1~2分
TEL 046-273-3307
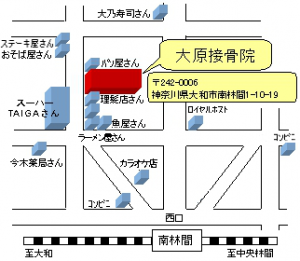
アクセス
南林間駅~大原接骨院までの道のり
診療時間
月)09:00 – 12:00 15:00 – 19:30
火)09:00 – 12:00 15:00 – 19:30
水)09:00 – 12:00 15:00 – 19:30
木)09:00 – 12:00 15:00 – 19:30
金)09:00 – 12:00 15:00 – 19:30
土)09:00 – 12:00 15:00 – 18:00
日)09:00 – 12:00
祝)09:00 – 12:00 15:00 – 18:00
定休日 なし